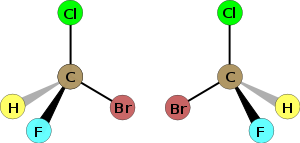
카이랄성 (화학)
카이랄성(영어: chirality)은 화학에서 거울상 영상에 서로 겹쳐질 수 없는 분자 구조를 나타내는 데 사용되는 용어이다. 분자 비대칭성(分子非對稱性), 키랄성, 손대칭성이라고도 한다.
사람의 손은 카이랄성을 설명하는 데 가장 쉬운 예제이다. 즉, 서로 거울에 비친 형태를 하고 있는 두 손의 경우, 두 손을 아무리 돌리고 방향을 바꾸고 하더라도 두 손은 서로 겹쳐지지 않는다. 따라서 카이랄성은 손대칭성이라고도 불리며, 카이랄성을 지닌 거울상 이성질체 혹은 광학 이성질체의 경우 이러한 오른손, 왼손에 비유하여 왼손잡이성(left-handedness) 내지는 오른손잡이성(right-handedness)으로 구분짓기도 한다. 두 거울상 이성질체가 동일한 양이 섞여있는 혼합물을 라세미 혼합물이라고도 한다. 분자구조에 있어서의 카이랄성은 입체화학에서 매우 중요한 특성이다.
역사
광학 활성도라는 말은 카이랄성을 지닌 물질이 편광에 대해 어떠한 반응을 보이는가를 설명하기 위해 도입되었다. 즉, (-) 형의 광학 이성질체의 용액은 편광면을 반시계 방향으로 회전시키며, (+) 형의 용액은 시계방향으로 회전시킨다. 이러한 편광면의 회전 현상은 1815년 장-밥티스테 비오가 처음으로 관찰하였다. 이후 광학 활성도는 설탕 제조 공정, 분석 화학, 약학 등에 많은 영향을 미쳤다. 1848년 루이 파스퇴르는 이러한 편광면의 회전 현상은 분자의 차이에 기인한 것이라는 것을 추론해내었다.
명명법
구조에 따른 명명법: R/S 명명법
R/S 명명법은 글리세르알데하이드와 같이 기준 분자가 없는 거울상 이성질체를 나타내는 데 주요하게 사용되는 명명법이다. R/S 명명법은 카이랄 중심에 붙어 있는 치환기를 원자 번호에 기반을 둔 칸-인골드-프렐로그 순위 규칙에 따라 우선 순위를 붙이고, 이에 따라 R 내지는 S라는 방식으로 표기를 하는 것이다. 우선, 카이랄 중심을 회전시켜, 4개 중에 가장 낮은 우선 순위를 지니는 치환기를 관측자 관점에서 먼 쪽으로 가도록 한다. 그러면 가장 낮은 우선 순위의 치환기는 카이랄 중심에 가려서 보이지 않게 되며, 나머지 3개의 치환기만이 보이게 된다. 이 상태에서 남은 3개의 치환기의 우선 순위가 오른쪽으로 감소하는지, 왼쪽으로 감소하는지를 따져서 구분짓게 된다. 오른쪽, 즉 시계방향으로 감소할 경우 R(오른쪽을 뜻하는 라틴어 Rectus), 반시계방향으로 감소할 경우 S(왼쪽을 뜻하는 라틴어 Sinister)로 구분짓는다.
이 방식을 사용하면, 분자의 각 카이랄 중심에 대해서 R이나 S로 구분지을 수 있다. 따라서 D/L 체계보다 훨씬 일반적으로, 부분입체이성질체와 같은 경우에 (R, R)과 (R, S)와 같이 구분할 수도 있다.
R/S 체계는 (+)/(-) 체계와 대응 관계가 존재하지 않는다. R 이성질체는 치환기에 따라 우회전성일수도, 좌회전성일수도 있다.
또한, R/S 체계는 D/L 체계와 대응 관계가 존재하지 않는다. 예로서, 세린의 곁사슬은 하이드록시기(-OH)를 지니고 있다. 만약 해당 하이드록시기가 싸이올기(-SH)로 치환된다면, D/L 명명법에 의한 분자명은 정의에 따라 치환에 영향을 받지 않는다. 하지만, 이러한 교환이 있게 된다면, 교환 전의 CH2OH는 CO2H 보다 우선순위가 낮은 반면 교환 후의 CH2SH는 CO2H 보다 우선순위가 높게 되어 R/S 명명법에 의한 분자식의 이름은 바뀌게 된다.
이러한 이유로, D/L 명명법은 아미노산이나 탄수화물을 다루는 일부 생화학 분야에서는 여전히 사용되고 있다. 이는 생명체에게서 흔히 발견되는 구조에게 동일한 이름을 부여하는 것이 보다 편리한 경우가 있기 때문이다. 다시말해, D/L 명명법을 사용한다면 일반적으로 생명체에서 발견되는 아미노산은 L-형으로 명명 가능하다. 하지만, R / S 명명법을 사용한다면, 비록 많은 수는 S형으로 명명 가능해도, 많은 예외가 발생하게 되는 것이다.
광학 활성도에 따른 명명법: (+)/(-) 명명법
거울상 이성질체는 편광면을 회전시키는 방향에 따라 구분지을 수도 있다. 빛의 진행방향에서 쳐다본 관측자에 있어 빛을 시계방향으로 회전시킨다면, 해당 거울상 이성질체는 (+)로 구분되고, 그에 반하는 분자는 (-)로 표시된다. (+) 와 (-) 이성질체는 우회전성(우선성)을 뜻하는 dextrorotatory와 좌회전성(좌선성)을 뜻하는 levorotatory로부터 각각 d-와 l-로 표기되기도 한다. 이러한 표기법은 아래의 D/L 표기법과 쉽게 혼동되므로 주의가 필요하다.
구조에 따른 명명법: D/L 명명법

거울상 이성질체는 원자의 부분적인 배치에 의해서 명명될 수도 있다.D/L 명명법은 분자를 글리세르알데하이드와 비교해서 명명하는 방법이다. 글리세르알데하이드는 자체로 카이랄성을 지니고 있으며, 두 개의 거울상 이성질체는 각각 D 와 L로 구분지어진다. 피셔 투영도 상에서 D-글리세르알데하이드의 하이드록시기는 오른쪽에, L-글리세르알데하이드에서는 왼쪽에 붙어 있다. 이와 유사하게 피셔 투영도 상에서 하이드록시기의 위치에 따라 D/L로 구분짓기도 한다. 따라서 그림과 같은 프럭토스의 두 거울상 이성질체는 구분된다.
D/L 표기법은 (+)/(−) 표기법 내지는 d/l 표기법과 관계가 없다. 즉, D가 반드시 d- 라거나 L 이 반드시 l- 인 것은 아니다. 단백질에서 흔히 발견되는 19개의 L-아미노산 중 9개는 d- 즉 우회전성이며, D-프럭토스는 다른 이름으로 l-프럭토스 즉 좌회전성이다.
일반적인 α-아미노산에 있어 D/L을 구분짓는 다른 방법은 일명 "CORN" 규칙을 적용하는 것이다. α-아미노산은 아미노기(-NH2), 카복시기(-COOH)가 하나의 탄소 원자에 붙어 있는 아미노산으로, 해당 탄소 원자가 입체중심으로 작용한다. 따라서 CORN 규칙은, 카이랄 중심인 탄소 주변에 카복시기(COOH), 치환기(R), 아미노기(NH2)의 순서를 따지는 것이다. 만약 수소 원자를 관측자에서 멀리 두었을때, 해당 순서가 시계방향이라면, D형 거울상 이성질체이며, 반시계방향이라면 L형 거울상 이성질체이다. 그림의 트레오닌에 있어 탄소 원자를 중심으로 카복시기, 치환기, 아미노기가 반시계 방향이므로, L-트레오닌이 된다.
생물학에서의 카이랄성
자연 발생하는 아미노산이나 당류를 비롯한 생물에서 사용되는 많은 분자는 카이랄성을 지닌다. 놀랍게도, 생물체에서 사용되는 화합물은 D/L 분류법으로 보았을 때, 대부분 같은 카이랄성을 지닌다. 대부분의 아미노산은 L형이며, 당류는 D형이다. 일반적으로 L형 아미노산을 이용해 자연적으로 형성되는 단백질은 왼손잡이성 단백질이라고 하며, D형 아미노산을 사용해 형성된 단백질은 오른손잡이성 단백질이라고 한다.
생물학에서 이러한 단일 카이랄성은 많은 논란의 대상이 되어왔다. 대부분의 과학자들은 지구 생명체의 이러한 카이랄성의 선택은 단순히 임의적으로 이루어진 것이며, 만약 탄소 기반의 외계 생명체가 존재한다면, 반대의 카이랄성을 지닐 수 있을 수도 있다고 한다. 하지만 일부 과학자들은 이러한 편향성에 대한 약한 상호작용과 같은 과학적인 이유를 찾고자한다.
효소 역시 카이랄성을 지니며, 카이랄성을 지닌 기질의 두 거울상 이성질체를 구분할 수 있다. 예로, 주머니처럼 생겨서 기질을 감싸안는 효소를 생각해보자. 만약 주머니의 구조가 대칭성이 아니라면, 기질의 형태에 따라 하나의 이성질체는 모양에 들어 맞는 반면, 다른 형태의 이성질체는 맞지 않을 것이다.
D형 아미노산은 단 맛이 나며, L형은 대개 무미하다. 스피어민트 잎과 캐러웨이 씨앗은 각각 L-카르본과 D-카르본을 지니고 있다. 이 두 분자는 서로 다른 향이 나며, 이 이유는 인간의 후각 기관이 거울상 이성질체에 서로 다르게 반응하는 카이랄 분자로 이루어져 있기 때문이다.
의약품에서의 카이랄성
카이랄성을 지니는 의약품은 쌍을 이루는 거울상 이성질체의 잠재적인 부작용을 방지하기 위해 높은 순도로 제조되어야 한다. 물론 쌍을 이루는 거울상 이성질체가 부작용이 있는 것이 아닌 단순히 효과가 없는 경우일 수도 있다.
- 탈리도마이드: 탈리도마이드는 라세미 혼합물이다. 하나의 거울상 이성질체는 조병에 효과가 있는 반면, 다른 거울상 이성질체는 기형아를 유발한다. 불행히도, 하나의 거울상 이성질체만을 정제하여 사용한다고 해도 기형을 억제할 수 있는 것은 아니다. 탈리도마이드는 인체 내부에서 쌍을 이루는 거울상 이성질체로 서로 변하게 되며, 따라서 한 종류의 이성질체만을 투여한다고 하더라도 인체 내부에는 두 종류의 탈리도마이드가 존재하게 된다.
- 에탐부톨: 한 종류는 결핵에 효과가 있는 반면, 다른 종류는 실명을 유발한다.
- 나프록센: 한 종류는 관절염 등에 효과가 있는 진통제인 반면, 다른 종류는 진통 효과도 없으며 간에 독성을 유발한다.
- 스테로이드 수용체는 입체 이성질체 특이성을 보인다.
- 페니실린의 작용은 입체선택성을 지닌다. 항생물질은 세균의 세포벽 내부에 존재하는 D-알라닌의 펩타이드 고리에만 작용한다. 하지만 인간은 이러한 D-아미노산을 가지고 있지 않기 때문에 페니실린을 사용하여 세균만을 죽일 수 있다.
- L-프로프라노롤은 강력한 아드레날린 수용체 차단제인 반면 D-프로프라노롤은 그렇지 않다. 하지만, 둘 모두 부분 마취 효과는 있다.
- 아드레날린 수용체와 반응하는 제제인 S(-) 카르베디롤은 R(+) 이성질체보다 100배 정도 베타 차단제로서 효과가 있다. 하지만 알파 차단제로서의 효과는 둘 모두 비슷하다.
무기 화학에서의 카이랄성
많은 배위 화합물은 카이랄성을 지니고 있다. 예로, 잘 알려진 [Ru(2,2'-bipyridine)3]2+착물은 3개의 바이피리딘 리간드가 카이랄 구조를 취하고 있다. 이 경우, 루테늄(Ru) 원자는 입체중심이 된다. 두 거울상 이성질체는 3개의 리간드의 방향에 따라 왼손잡이성일경우 Λ, 오른손잡이성일경우 Δ으로 표기된다.
아민의 카이랄성
그림과 같은 삼차 아민은 탄소 화합물과 유사하게 카이랄성을 지니고 있다. 즉 고립전자쌍까지 고려한다면, 중앙의 질소 원자에 네 개의 치환기가 달려있는 형태인 것이다. 하지만, 입체중심의 질소 반전에 필요한 에너지 장벽은 대략 30 kJ/mol 정도로, 상온에서 두 이성질체는 서로 빠른 속도로 변환될 수 있다. 결과적으로, NHRR' 형태의 아민은 광학적으로 구분될 수 없으며, NRR'R" 형태의 아민이라 하더라도 R, R', R"의 치환기가 순환 구조일 때만 구분될 수 있다.
문학에서의 카이랄성
루이스 캐럴의 생전에는 카이랄성이 그다지 연구된 것은 아니었지만, 《거울 나라의 앨리스》에서 앨리스가 고양이에게 "거울에 비친 우유는 몸에 나쁠거야" 라며 거울상 물질의 생물학적 차이에 대한 추측을 하였다.
제임스 블리시의 《스타 트렉》소설인 《Spock Must Die!》에서는 거울상의 스팍이 등장하는데, 거울상으로 되어버린 물질대사로 인해 거울상 이성질체인 아미노산을 합성해서 사용하는 장면이 등장한다.
참조 문헌
외부 링크
- http://www.chemguide.co.uk/basicorg/isomerism/optical.html#top
- http://www.nature.com/horizon/chemicalspace/highlights/s5_nonspec1.html
- IUPAC nomenclature for amino acid configurations.
- Michigan State University's explanation of R/S nomenclature
- Quack: Chiral Skin Care by Charlatans, from Melbourne Dermatology Online